Trump vai anunciar tarifas sobre produtos farmacêuticos nas próximas duas semanas
O Presidente dos Estados Unidos, Donald Trump, adiantou segunda-feira que vai anunciar tarifas sobre produtos farmacêuticos “nas próximas duas semanas”, depois de ter assinado uma ordem executiva para promover o fabrico destes produtos em solo norte-americano.
Infarmed suspende ativididade do distribuidor CannaPhytica
A Autoridade Nacional do Medicamento (Infarmed) alerta que os medicamentos distribuídos pela CannaPhytica não devem ser comercializados em Portugal, na sequência da suspensão da atividade deste distribuidor alemão.

Portugal Inicia Campanha de Vacinação Sazonal 2024-2025: 3 Milhões de Doses Prontas para Distribuição
A operação logística, que começou hoje, visa distribuir 3 milhões de doses de vacinas contra a gripe e a COVID-19 por todo o território nacional, numa demonstração impressionante de eficiência e preparação do sistema de saúde português.

Farmacêuticos Hospitalares: pilares invisíveis do SNS na vanguarda dos cuidados de saúde
O trabalho do Farmacêutico Hospitalar começa muito antes do medicamento chegar ao doente, garantindo que se encontrem disponíveis no hospital os medicamentos certos para cada tratamento
GSK anuncia resultados positivos do ensaio clínico de fase III de mepolizumab para a DPOC
A gigante farmacêutica GSK plc anunciou hoje resultados altamente promissores do seu ensaio clínico de fase III, denominado MATINEE, que avalia a eficácia do mepolizumab no tratamento da Doença Pulmonar Obstrutiva Crónica (DPOC)

Estudo estima mais de 39 milhões de mortes até 2050 por infeções resistentes a antibióticos
Mais de 39 milhões de pessoas podem morrer nos próximos 25 anos no mundo devido a infeções bacterianas resistentes a antibióticos, estima um estudo hoje divulgado na revista médica britânica The Lancet.
Dovato demonstra eficácia equivalente e menor ganho de peso face ao Biktarvy no tratamento do VIH-1
A ViiV Healthcare, empresa líder mundial especializada em VIH, anunciou hoje resultados promissores do estudo PASO DOBLE, que compara a eficácia de dois regimes de tratamento para o VIH-1.

Projeto Saúde Mental 360º Algarve Promove Sessão sobre Segurança dos Medicamentos em Olhão
O Projeto Saúde Mental 360º Algarve, uma iniciativa da Plataforma Saúde em Diálogo, irá realizar uma sessão informativa intitulada “Segurança dos medicamentos: tod@s podemos contribuir!” no próximo dia 20 de setembro de 2024, pelas 14h30, no Auditório da Biblioteca Municipal de Olhão.
Professor Marian Galovic: “o impacto da epilepsia na estrutura e função do cérebro humano”
Ao Professor Doutor Marian Galovic, Doutorado em Medicina e Investigador na Universidade de Zurique, na Suíça, coube a segunda comunicação no simpósio Angelini, dedicado ao tema “Crises geram mais do que crises: O impacto da epilepsia não controlada.”
Simpósio Angelini: Crises geram mais do que crises: O impacto da epilepsia não controlada.
Segundo Adam Strzelcz, os custos indiretos representam cerca de 3/4 de todos os custos associados à epilepsia, destacando-se o impacto significativo da doença na capacidade dos indivíduos de participarem da força de trabalho.
Evitar o Excesso de Tratamento e o Niilismo Terapêutico na Epilepsia
No 15º Congresso Europeu sobre Epilepsia, o Professor Steinhoff enfatizou que o cenário perfeito seria aquele composto por uma equipa duradoura e confiável de médico, doente e familiares
Professor Vicente Villanueva: O uso precoce de Cenobamato permite melhores resultados na epilepsia
É claro que devemos fazer algo diferente, pelo menos para nos movermos um pouco mais rápido para aqueles doentes que sabem que não estão a ter bons resultados.
O Impacto dos Novos Medicamentos no Tratamento da Epilepsia Refratária e na Via Cirúrgica da Epilepsia
Em Roma, a Professora Samarasekera apresentou dados de uma coorte de 143 doentes em Birmingham, dos quais um terço apresentava deficiência intelectual e alguns, epilepsias geneticamente mediadas
Superando Barreiras para a Liberdade de Crises na Epilepsia: Conciliando Teoria e Prática
Este simpósio, patrocinado pela Angelini, decorreu no segundo dia do 15º Congresso Europeu sobre Epilepsia, organizado pela Liga Internacional Contra a Epilepsia (ILAE) Europa, que teve lugar em Roma de 7 a 11 do corrente.

Infarmed manda retirar do mercado um lote do medicamento Lorazepam
A autoridade nacional do medicamento (Infarmed) ordenou a suspensão imediata de um lote do medicamento Lorazepam, indicado no tratamento da ansiedade, devido à deteção de um resultado irregular num estudo de estabilidade.
Medicamento para a perda de peso reduz significativamente IMC em crianças obesas
Os resultados deste estudo, foram divulgados no EASD Annual Meeting 2024, que decorre até amanhã em Madrid.

EMA aprovou a seringa pré-cheia para a administração de Eylea na UE
A Agência Europeia de Medicamentos (EMA) aprovou a seringa pré-cheia para a administração de Eylea ™ 8 mg (solução injetável de 114,3 mg/ml) na União Europeia. A nova seringa pré-cheia OcuClick ™ permitirá aos oftalmologistas administrar com precisão a dose de 70 microlitros de Eylea™ 8 mg para as indicações aprovadas de degenerescência macular da idade neovascular (DMIn) (húmida) e edema macular diabético (EMD) de uma forma simples e eficiente. A Alemanha será um dos primeiros mercados a lançar a a seringa pré-cheia.
Cenobamato mostra resultados promissores no tratamento da epilepsia focal
A análise post-hoc do estudo C021 revelou elevadas taxas de retenção ao terceiro ano, independentemente das categorias etiológicas, variando entre 60,3% e 77,9%.
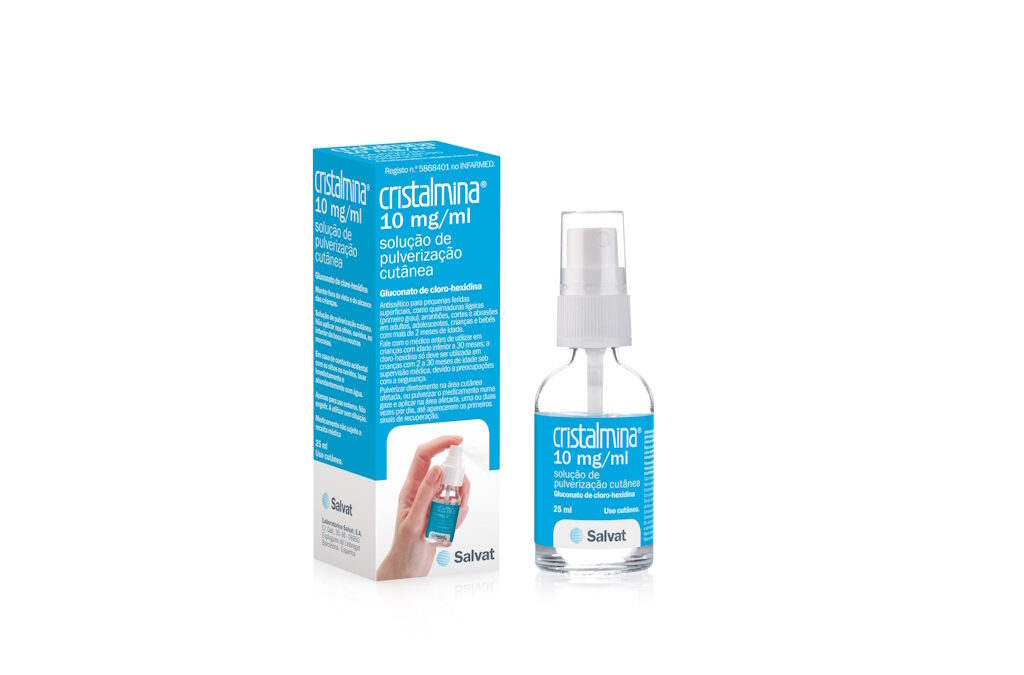
Laboratórios Salvat lançam Cristalmina®, o primeiro medicamento transparente para feridas e queimaduras ligeiras em Portugal
Os Laboratórios Salvat, companhia farmacêutica independente, acabam de lançar em Portugal Cristalmina®, um medicamento antissético à base de clorhexidina (10mg/ml) indicado para o tratamento de pequenas feridas superficiais e queimaduras ligeiras (primeiro grau).
Comissão Europeia aprova efanesoctocog alfa da Sobi® para o tratamento da hemofilia A
Novo medicamento oferece proteção elevada contra hemorragias com uma dose única semanal

Politécnico da Guarda quer transformar pasta de papel em cápsula de medicamentos
A nova unidade de investigação do Instituto Politécnico da Guarda (IPG) quer utilizar um subproduto da indústria do papel para encapsular fármacos, nomeadamente agentes terapêuticos anticancerígenos, anti-inflamatórios ou ansiolíticos, anunciou hoje aquela instituição de ensino.
AbbVie submete pedido de aprovação de upadacitinib para arterite de células gigantes à FDA e EMA
A AbbVie anunciou a submissão de pedidos de autorização de introdução no mercado (AIM) à FDA (Food and Drug Administration) e à Agência Europeia de Medicamentos (EMA) para o upadacitinib (15 mg, uma vez por dia) no tratamento de doentes adultos com arterite de células gigantes (ACG).
Bayer inicia ensaio de fase III para cancro do pulmão de não-pequenas células
Bayer inicia ensaio de fase III para novo fármaco contra cancro do pulmão de não-pequenas células com mutação HER2, visando terapêutica personalizada.

Nanopartículas abrem caminho para testes de stress em casa
O stress assume várias formas no nosso quotidiano, desde as exigências implacáveis do trabalho até à correria constante das idas à escola. No entanto, ignorar níveis elevados de stress pode levar a problemas de saúde graves, como depressão e doença de Alzheimer. E se...
Semaglutida reduz mortes relacionadas com a COVID-19 em pacientes com obesidade e doenças cardiovasculares
A capacidade da semaglutida para reduzir significativamente os eventos adversos cardiovasculares e relacionados com a COVID-19 sublinha o potencial transformador de abordar a obesidade e melhorar a saúde cardiometabólica como uma estratégia para proteger contra uma ampla gama de ameaças à saúde.
Submetido pedido de autorização de novo medicamento para sintomas vasomotores associados à menopausa
A Bayer anunciou hoje que foi submetido um pedido de autorização de novo medicamento (NDA), para o medicamento experimental elinzanetant, à Autoridade dos Alimentos e Medicamentos (FDA) para o tratamento de sintomas vasomotores (SVM, também conhecidos como afrontamentos) moderados a graves associados à menopausa. A submissão tem por base os resultados positivos dos estudos de Fase III OASIS 1, 2 e 3.
ÚLTIMAS
Diploma português transpõe diretiva europeia sobre 2-metiloxolano e altera legislação nacional
O Presidente da República promulgou hoje o diploma que transpõe para a ordem jurídica nacional a Diretiva (UE) 2023/175, relativa ao 2-metiloxolano, alterando o Decreto-Lei n.º 304/98, de 7 de outubro, reforçando a regulação do uso deste solvente em Portugal.
Infeções por VIH no menor número desde 1980, mas metas para 2025 em atraso
O número de novas infeções pelo vírus da imunodeficiência humana (VIH) em 2023 foi o menor desde o final dos anos 1980, assinalou a ONU, embora alertando que o mundo está atrasado no cumprimento das metas para 2025.
Angola e Moçambique entre países que se comprometem a eliminar a cólera até 2030
Vinte países africanos, nomeadamente os lusófonos Angola e Moçambique, comprometeram-se a eliminar a cólera até 2030, após uma reunião ‘online’ organizada pela União Africana, anunciou hoje a entidade num comunicado.
Técnicos auxiliares de saúde da Madeira em greve na sexta-feira por melhores salários
Os técnicos auxiliares de saúde da Madeira vão estar em greve na sexta-feira, reivindicando a valorização da carreira e aumento dos salários, indicou hoje o Sindicato dos Trabalhadores em Funções Públicas e Sociais do Sul e Regiões Autónomas (STFPSSRA).
Satisfação dos profissionais de saúde aumenta em função de cargo, idade e condições de Trabalho – estudo
A satisfação dos médicos e enfermeiros dos setores público e privado aumenta quando ocupam cargos de chefia, são mais velhos, têm horários fixos e trabalham em exclusividade, revela hoje um estudo nacional.
APH apresenta novo site com imagem renovada e navegação intuitiva
A Associação Portuguesa de Hemofilia e de outras Coagulopatias Congénitas (APH) lançou um novo website, com design moderno, navegação intuitiva e recursos atualizados, reforçando o apoio à comunidade e facilitando o acesso à informação essencial.
MAIS LIDAS
-
Saúde e Trabalho: a propósito de uma canção italiana de trabalho do séc. XIX
Provavelmente uma canção de trabalho italiana do final do século XIX, a Bella Ciao, terá sido desenvolvida no trabalho agrícola em arrozais. Entre nós, também [...] -
O que se exigia a trabalhadora(e)s! e não foi assim há tanto tempo …
Não decorreram assim tantos anos quanto se poderia pensar da época em que se impunham medidas laborais com grande impacto na vida da(o)s trabalhadora(e)s. Recentemente adquiri, [...] -
Associações improváveis: Presidentes da República e acidentes de trabalho!
A propósito da “telenovela” noticiosa do (des)convite do Presidente Jair Bolsonaro ao nosso Presidente Marcelo Rebelo de Sousa que “canibalizou” os canais noticiosos deste “rectangulozinho [...]

